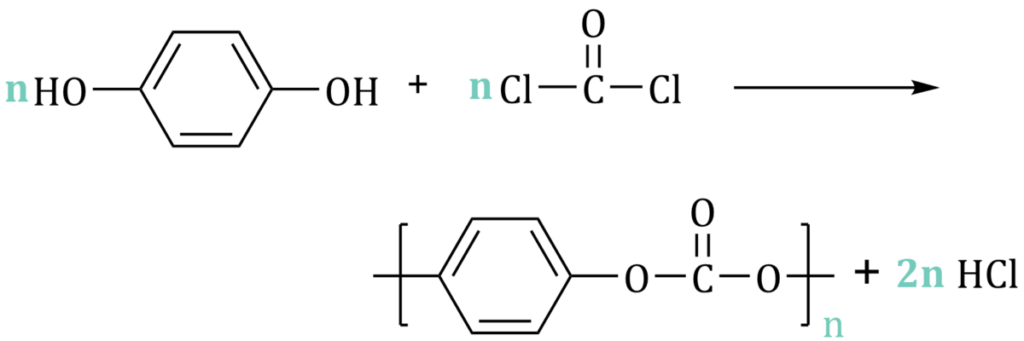Polimeryzacja – jak z małych cząsteczek powstają duże cząsteczki?
Polimery są wszędzie – od plastikowych butelek, przez opakowania, aż po ubrania i części samochodów.
W tym artykule przeprowadzimy Cię krok po kroku przez zagadnienie polimeryzacji – zgodnie z wymaganiami podstawy programowej – tak by ustalanie wzorów monomerów i polimerów oraz zapis odpowiednich równań reakcji nie stanowił dla Ciebie problemu.
Co to jest polimeryzacja?
Polimeryzacja to reakcja chemiczna, w której wiele małych cząsteczek (nazywanych monomerami) łączy się ze sobą w jeden długi łańcuch, tworząc polimer.
Wyobraź sobie monomery jak klocki LEGO – pojedynczo niewiele znaczą, ale po połączeniu tworzą imponujące konstrukcje.
Rodzaje polimeryzacji
Reakcje polimeryzacji, ze względu na mechanizm, dzieli się na dwa podstawowe typy: polimeryzację addycyjną
i polimeryzację kondensacyjną.
Polimeryzacja addycyjna (łańcuchowa) jest to proces, w którym nie powstają produkty uboczne.
W ten sposób z etenu (CH₂=CH₂) powstaje polietylen (PE, -[CH2-CH2]n-).
Polimeryzacja kondensacyjna (polikondensacja) jest to proces, w którym monomery łączą się ze sobą
z wydzieleniem małych cząsteczek, np. wody. Na drodze polikondensacji otrzymuje się między innymi, poliestry i poliamidy.
Jak napisać równanie reakcji polimeryzacji?
Na początku należy ustalić z jakim typem polimeryzacji mamy do czynienia. Jeżeli monomerem jest związek organiczny z wiązaniem nienasyconym (alken, dien, alkin) to ulegnie on reakcji polimeryzacji addycyjnej.
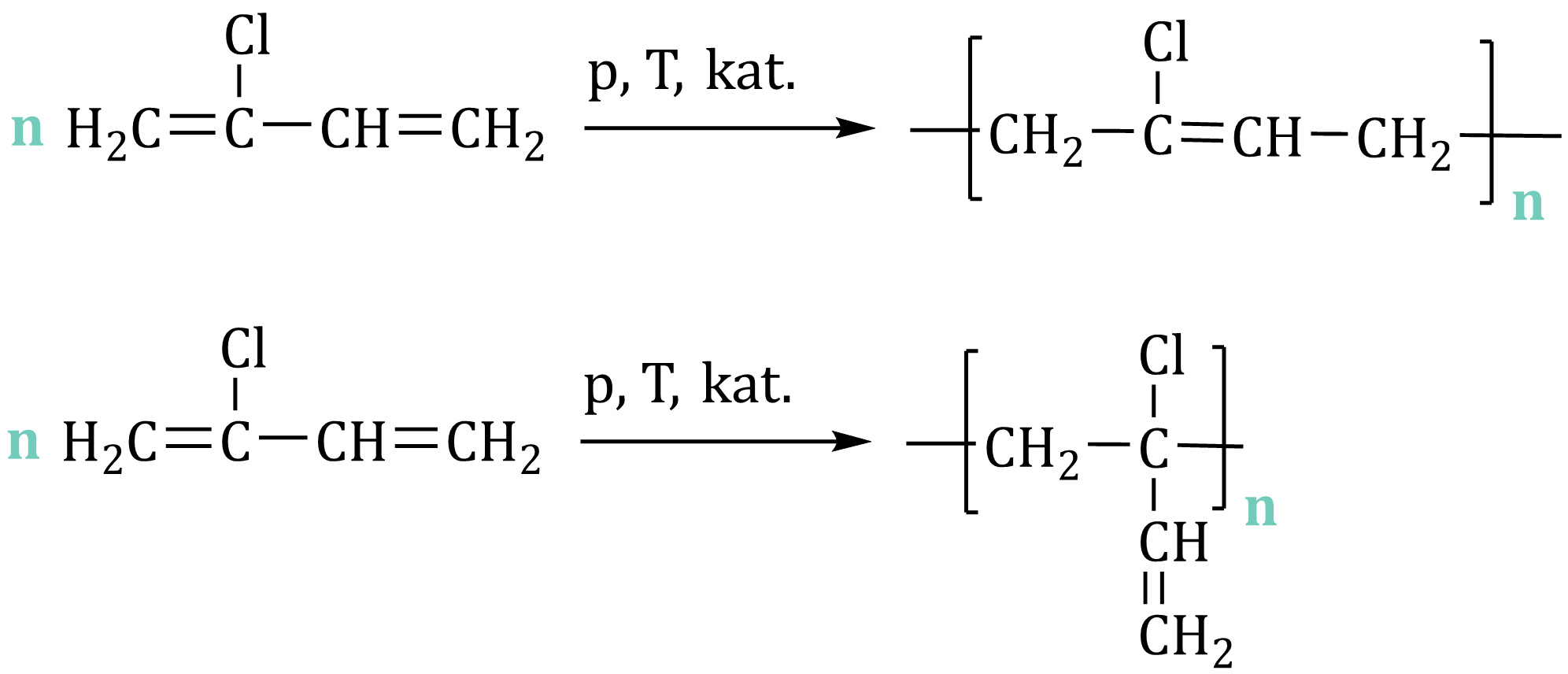
Poniżej przedstawiono reakcję polimeryzacji chlorku winylu, w wyniku której otrzymujemy poli(chlorek winylu), PCV – używany np. do rur, wykładzin czy okien.

Innym przykładem może być reakcja polimeryzacji 2-chlorobuta-1,3-dienu prowadząca do polichloroprenu (kauczuku syntetycznego). Polimeryzacja takiego monomeru może przebiegać w położeniach 1, 4 lub 1, 2. W pierwszym przypadku powstają makrocząsteczki o nienasyconych łańcuchach liniowych, w drugim przypadku łańcuch główny polimeru nie zawiera podwójnych wiązań, natomiast występują one w łańcuchach bocznych.
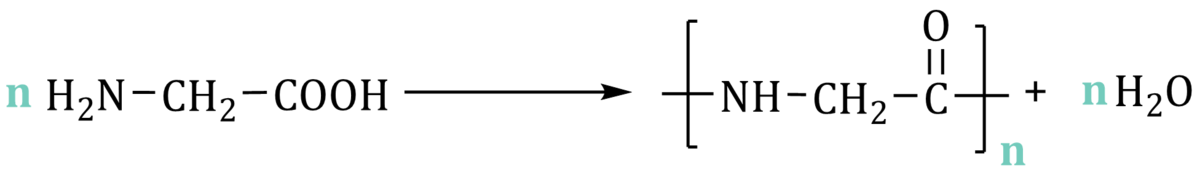
Gdy amina reaguje z kwasem karboksylowym w wysokiej temperaturze, z wydzieleniem cząsteczki wody, powstaje amid. Gdy n cząsteczek aminokwasu ulegnie reakcji powstanie poliamid składający się z n merów. Na przykładzie równania reakcji polimeryzacji glicyny:
Poliamidy otrzymuje się również w wyniku reakcji diaminy z kwasem dikarboksylowym. Każda z tych cząsteczek może utworzyć przynajmniej dwa wiązania amidowe, łącząc ze sobą coraz więcej cząsteczek aż powstanie ogromna cząsteczka poliamidu. Na rysunku poniżej indeksy m i l oznaczają ilość grup CH2 w poszczególnych monomerach.
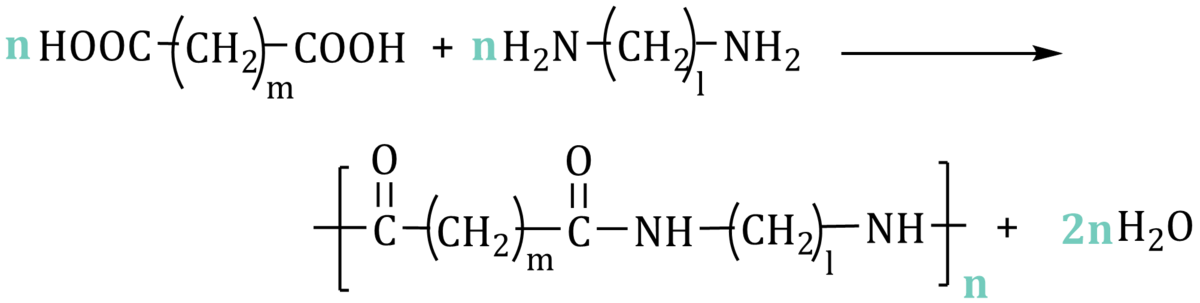
Reakcje takie przeprowadza się zwykle używając zamiast kwasu dikarboksylowego, jego znacznie bardziej reakctywnej pochodnej – chlorku kwasu dikarboksylowego. Chlorków kwasów karboksylowych nie ma w postawie programowej do matury z chemii. Poniższa reakcja pojawia się w tym artykule po to, aby pokazać, że w wyniku polikondensacji może wydzielić się nie tylko woda, ale np. HCl czy NaCl.
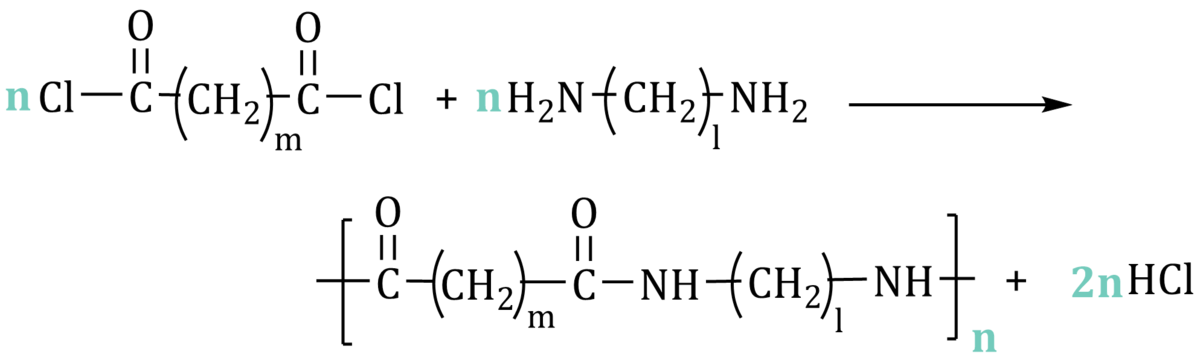
Jeżeli zamiast diaminy, z cząsteczkami kwasu dikarboksylowego zareagują cząsteczki diolu powstanie poliester.
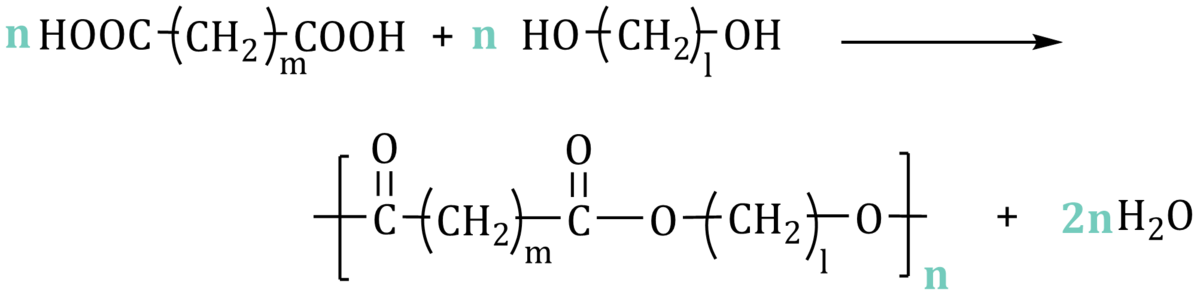
Jak rozpoznać mer w polimerze?
Mer w polimerze to podstawowy fragment struktury chemicznej, który powtarza się wielokrotnie w łańcuchu polimerowym. Aby rozpoznać mer w strukturze polimeru, należy wykonać następujące kroki:
- Zidentyfikuj fragmenty powtarzające się w łańcuchu, fragmenty te muszą zawierać wiązanie węgiel-węgiel.
- Sprawdź, czy ten fragment ma „wolne końce” do dalszego łączenia.
- Wyodrębnij go jako mer.
Na przykładzie polietylenu: -[CH2-CH2]n– mer to: –CH₂–CH₂–
Jak rozpoznać z jakiego monomeru powstał polimer?
Rozpoznanie, z jakiego monomeru powstał dany polimer, polega na odwróceniu procesu polimeryzacji — należy „rozłożyć” polimer do podstawowych jednostek, czyli zobaczyć, co było jego źródłem.
Jak to zrobić:
1. Zidentyfikuj jednostkę powtarzalną (mer)
2. Zastanów się, co trzeba „dodać”, by wrócić do monomeru. Należy tu zidentyfikować rodzaj polimeryzacji.
🔹 Polimeryzacja addycyjna (łańcuchowa)
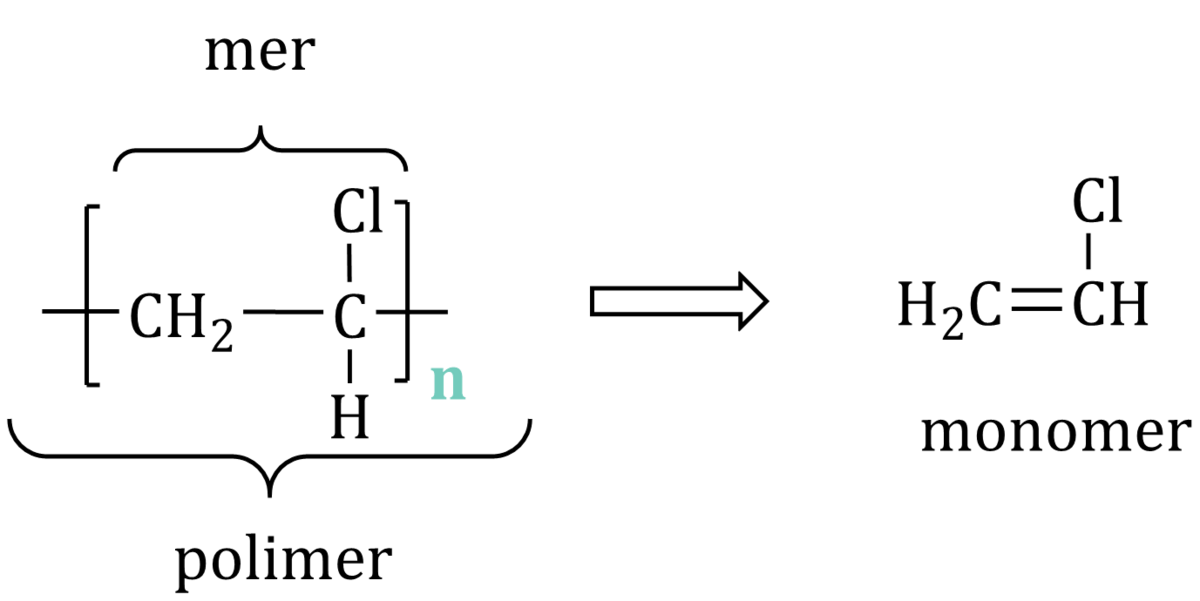
- Zachodzi przez „rozerwanie” wiązania podwójnego w monomerze (np. CH₂=CHX).
- MER ma wtedy strukturę nasyconą (bez wiązań podwójnych), ale monomer miał wiązanie podwójne.
🔹 Polimeryzacja kondensacyjna (ze związków bifunkcyjnych)
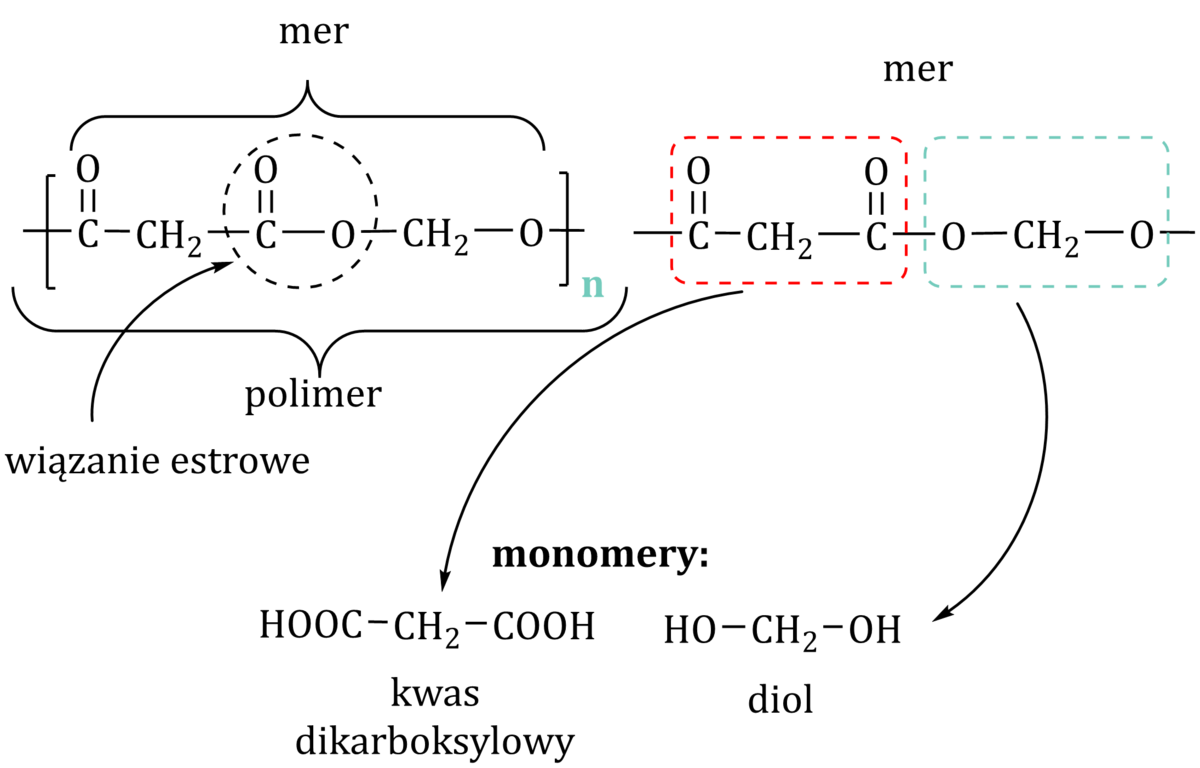
- MER zawiera wiązania estrowe, amidowe itp.
- Trzeba „rozciąć” wiązania funkcyjne i „dodać” grupy końcowe, które powstają podczas kondensacji (np. -OH, -NH₂, -COOH).
Zadania w stylu maturalnym
Zadanie 1.
Poniżej przedstawiono wzór pewnego polimeru.
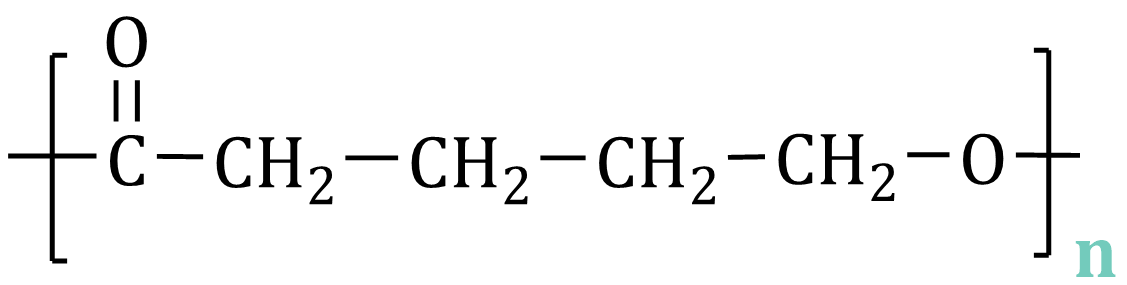
Podaj nazwę systematyczną monomeru z którego postał ten polimer oraz ustal rodzaj polimeryzacji.
Nazwa monomeru:
Rodzaj polimeryzacji:
Odpowiedź:
Nazwa monomeru: kwas 5-hydroksypentanowy
Rodzaj polimeryzacji: polikondensacja
Zadanie 2.
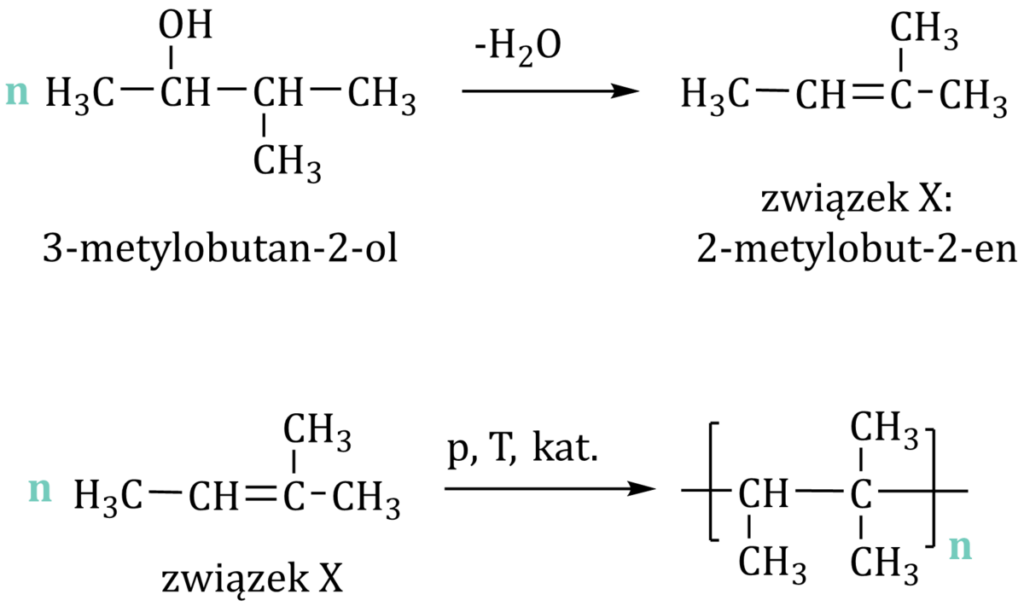
3-metylobutan-2-ol poddano reakcji z KOH w wysokiej temperaturze, w wyniku której powstał związek X. Związek ten następnie uległ polimeryzacji.
Podaj nazwę systematyczną związku X oraz ustal wzór polimeru.
Nazwa systematyczna związku X:
Wzór polimeru:
Odpowiedź:
Nazwa systematyczna związku X: 2-metylobut-2-en
Wzór polimeru:
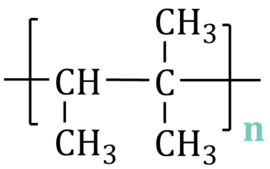
Komentarz:
Zadanie 3.
Poliwęglany są formalnie zaliczane do estrów kwasu węglowego.
Uzupełnij schemat tak, aby przedstawiał syntezę poliwęglanu z 1,4-dihydroksybenzenu oraz fosgenu. Fosgen to silnie trujący związek o wzorze COCl2. W reakcjach fosgenu z alkoholami otrzymuje się odpowiednie estry kwasu węglowego.

Odpowiedź: